已知某原电池的正极是氢电极P(H2)=100kPa,负极的电极电势是恒定的,当氢电极中pH=4.008时,该电池
已知某原电池的正极是氢电极P(H2)=100kPa,负极的电极电势是恒定的,当氢电极中pH=4.008时,该电池的电动势为0.412V;如果氢电极中所用的溶液为—未知c(H+)的缓冲溶液,又重新测得原电池的电动势为0.427V。计算缓冲溶液的H+浓度和pH。若缓冲溶液中f(HA)=c(A—)=1.0mol.L—1,求该弱酸HA的解离常数。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
已知某原电池的正极是氢电极P(H2)=100kPa,负极的电极电势是恒定的,当氢电极中pH=4.008时,该电池的电动势为0.412V;如果氢电极中所用的溶液为—未知c(H+)的缓冲溶液,又重新测得原电池的电动势为0.427V。计算缓冲溶液的H+浓度和pH。若缓冲溶液中f(HA)=c(A—)=1.0mol.L—1,求该弱酸HA的解离常数。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知某原电池的正极是氢电极P(H2)=100kPa,负极的电…”相关的问题
更多“已知某原电池的正极是氢电极P(H2)=100kPa,负极的电…”相关的问题
第1题
已知某原电池的正极是氢电极,p(H2)为100kPa,负极的电极电势是恒定的。当氢电极中pH=4.008时,该电池的电动势是0.412V。如果氢电极中所用的溶液改为一未知c(H+)的缓冲溶液,又重新测得原电池的电动势为0.427V。计算该缓冲溶液的H+浓度和pH值。如该缓冲溶液中c(HA)=c(A-)=1.0mol·dm-3,求该弱酸HA的电离常数。
第2题
第3题
第4题
将氢电极插入含有0.50mol·dm-3HA和0.10mol·dm-3A-的缓冲溶液中,作为原电池的负极;将银电极插入含有AgCl沉淀和1.0mol·dm-3Cl-的溶液中。已知p(H2)=100kPa时测得原电池的电动势为0.450V,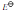 (Ag+/Ag)=0.7996V。
(Ag+/Ag)=0.7996V。

第5题
第6题
由两个氢电极Pt|H2(100kPa)|H+(0.10mol·dm-3)和Pt|H2(100kPa)|H+(xmol·dm-3)组成的原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,问组成该电极的溶液中的H+的浓度x值为多少?
第7题
12.由两个氢电极H2(100kPa)|H+(0.10mol·dm-3)|Pt和H2(100kPa)|H+(xmol·dm-3)|Pt组成原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,求组成该电极的溶液中H+的浓度x的值。
第8题
第9题
由两个氢电极H2(100kPa)|H+(0.10mol·dm-3)|Pt和H2(100kPa)|H+(xmol·dm-3)|Pt组成原电池,测得该原电池的电动势为0.016V。若后一电极作为该原电池的正极,求组成该电极的溶液中H+的浓度x的值。
第10题
,测得E=1.050V,取此NaOH溶液20.00cm3,需上述HCl溶液多少立方厘米时才能完全中和? (已知25℃时,标准甘汞电极的电极电势为0.2828V,p(H2)=105Pa)


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧