已知反应2H2(g)+2NO(g)→2H2O(g)+N2(g)的速率方程υ=kc(H2)·c2(NO),在一定温度下,若使容器体积缩小到原来的1/
已知反应2H2(g)+2NO(g)→2H2O(g)+N2(g)的速率方程υ=kc(H2)·c2(NO),在一定温度下,若使容器体积缩小到原来的1/2时,问反应速率如何变化?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
已知反应2H2(g)+2NO(g)→2H2O(g)+N2(g)的速率方程υ=kc(H2)·c2(NO),在一定温度下,若使容器体积缩小到原来的1/2时,问反应速率如何变化?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知反应2H2(g)+2NO(g)→2H2O(g)+N2(g…”相关的问题
更多“已知反应2H2(g)+2NO(g)→2H2O(g)+N2(g…”相关的问题
第1题
已知反应:2NO(g)+2H2(g)=N2(g)+2H2O(g)的反应历程为:
①2NO(g)+H2(g)→N2(g)+H2O(g)(慢反应)
②H2O2(g)+H2(g)=2H2O(g)(快反应)
则此反应称为()反应。此两步反应均称为()反应,而反应①称为总反应的(),总反应的速率方程式为(),此反应为()级反应。
第2题
已知反应2NO(g)+2H2(g)→N2(g)+2H2O(g),其速率方程对NO(g)是二次方程、对H2(g)是一次方程。
(1)写出N2生成的速率方程。
(2)如果浓度以mol·L-1表示,反应速率常数k的单位是什么?
(3)写出NO浓度减小的速率方程,这里的速率常数k和(1)中的k的值是否相同,两个k值间的关系是怎样的?
第3题
反应2NO(g)+2H2(g)→N2(g)+2H2O(g),其速率方程式中对[NO]是二次幂,对[H2]是一次幂。

第4题
化学反应2NO(g)+2H2(g)=N2(g)+2H2O(G)的反应机理如下:
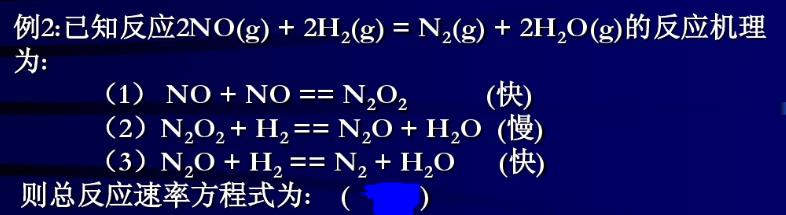
试写出总反应的速率方程。
第5题
在1073K时发生如下反应:2H2(g)+2NO(g)=N2(g)====2H2O(g)
为了确定反应的速率方程,通过配制一系列NO (g)与H2(g)浓度不同的混合物,测定反应起始速率,有关实验数据见下表,求该反应的速率方程。
H2(g)和NO(g)的反应速率(1073K)
| 实验标号 | 起始浓度/mol·dm-3 | 形成N2(g)的起始速率 /mol·dm-3·s-1 | |
| c(NO) | c(H2) | ||
| 1 2 3 4 5 6 | 6.0×10-3 6.0×10-3 6.0×10-3 1.0×10-3 2.0×10-3 3.0×10-3 | 1.0×10-3 2.0×10-3 3.0×10-3 6.0×10-3 6.0×10-3 6.0×10-3 | 3.19×10-3 6.36×10-3 9.56×10-3 0.48×10-3 1.92×10-3 4.30×10-3 |


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧