随后转化步骤是一个可逆的电极反应紧接着一个不可逆的化学反应,因此与电极可逆反应的极化曲线相比,其阴极极化曲线整体向负电势方向移动。()
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“随后转化步骤是一个可逆的电极反应紧接着一个不可逆的化学反应,…”相关的问题
更多“随后转化步骤是一个可逆的电极反应紧接着一个不可逆的化学反应,…”相关的问题
第1题
A.可逆电池必须由可逆电极组成
B.可逆电池的电池反应必须可逆
C.无液体接界的单液电池为可逆电池
D.由可逆电极组成的电池,电池的电动势最大
E.电极反应可逆时组成的电池一定是可逆电池
第4题
以Ni(s)为电极、KOH水溶液为电解质的可逆氢、氧燃料电池,在298 K和标准压力下稳定地连续工作,试回答下述问题。
(1)写出该电池的表达式、电极反应和电池反应。
(2)求一个100 W(1 W=3.6kJ·h-1)的电池,每分钟需要供给298 K、100 kPa压力的H2(g) ;的体积。已知该电池反应每消耗1 mol H2(g)时的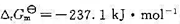 .
.
(3)该电池的电动势为多少?
第5题
101.3kPa,25℃下,下列反应的反应焓为5.36kJ·mol-1:
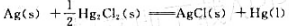
已知25℃时,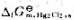 =-210.7kJ·mol-1,
=-210.7kJ·mol-1,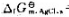 =-109.7kJ·mol-1,请:
=-109.7kJ·mol-1,请:
(1)试为上述反应设计一可逆电池,写出电池表示式和电极反应;
(2)求所设计电池的电动势及其温度系数和电池反应的ΔtGmθ、ΔtSmθ:
(3)求25℃时,电极C1-|Hg2Cl2|Hg的标准电极电位;
已知25℃时,Eθ[Ag+|AgCl(s)|Ag]=0.2224V
(4)已知25℃时Eθ(Hg22+|Hg)=0,798V,求Hg2Cl2在25℃时的溶度积.
第9题
298K时,反应H2(g)+Ag2O(s)====2Ag(s)+H2O(l)的恒容热效应QV=-252.79kJ·mol-1。在298K、标准压力下,将上述反应体系构成一可逆原电池,则其电动势的温度系数为-5.044×10-4V·K-1。求Ag(s)|Ag2O(s)|OH-电极的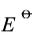 。已知298K时水的离子积Kw=1×10-14。
。已知298K时水的离子积Kw=1×10-14。
第10题
A.交换电流密度大,难极化,电极反应可逆性大
B.交换电流密度小,难极化,电极反应可逆性大
C.交换电流密度趋近于0,理想不极化电极,电极反应完全可逆
D.交换电流密度趋近于无穷大,理想极化电极,电极反应完全不可逆


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧