已知298K时下列两个反应的平衡常数: 试求反应在该温度下的平衡常数。
已知298K时下列两个反应的平衡常数:
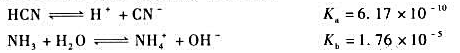
试求反应 在该温度下的平衡常数。
在该温度下的平衡常数。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
已知298K时下列两个反应的平衡常数:
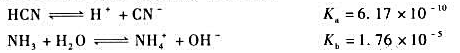
试求反应 在该温度下的平衡常数。
在该温度下的平衡常数。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知298K时下列两个反应的平衡常数: 试求反应在该温度下的…”相关的问题
更多“已知298K时下列两个反应的平衡常数: 试求反应在该温度下的…”相关的问题
第2题
已知298K时,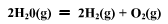 反应的平衡常数为9.7×10-81,这时H2O(1)的饱和蒸气压为3200Pa,试求298K时下述电池的电动势E。
反应的平衡常数为9.7×10-81,这时H2O(1)的饱和蒸气压为3200Pa,试求298K时下述电池的电动势E。
Pt|H2(P3)|H2SO4(0.01mol·kg-1)|O2(P3)|Pt
(298K时的平衡常数是根据高温下的数据间接求出的。由于氧电极上反应不易达到平衡,不能测出E的精确值,所以可通过此法来计算E值。)
第3题
已知反应:

298K时的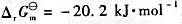 。试计算:
。试计算:
(1)该反应的标准平衡常数 ;
;
(2)若空气中H2S的分压为3.1Pa,试计算可以确保铜单质免遭H2S腐蚀时H2的分压。
第5题
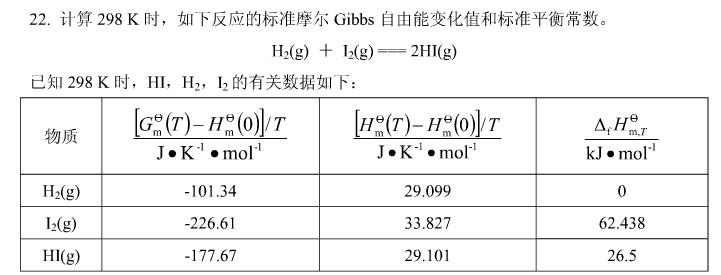
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知298K时,HI、H2、I2的有关数据如下:
第6题
298K时,已知
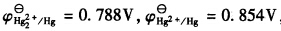 ,试计算:(1)反应Hg2++2e→
,试计算:(1)反应Hg2++2e→
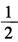 Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
Hg22+的标准电极电势;(2)为反应Hg+Hg2+→Hg22+设计电池,并计算该反应的标准平衡常数。
第9题
已知在298K时,下列反应:
①CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s),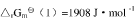
②
③C(石墨)+O2(g)===CO2(g),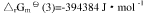
④N2(g)+3H2(g)===2NH3(g),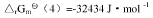 试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能
试求:(1)尿素CO(NH2)2(s)的标准摩尔生成Gibbs自由能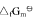 ;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数
;(2)由稳定单质生成尿素反应的平衡常数与上列反应平衡常数的关系式;(3)由单质生成尿素反应的平衡常数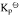 。
。
第10题
已知反应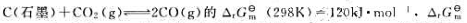 (1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。
(1000K)=-3.4kJ·mol-1,计算(1) 在标准状态及温度分别为298K和1000K时的标准平衡常数;(2)当1000K时,p(CO)=200kPa,p(CO2)=800kPa,判断该反应方向。


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧