题目内容
(请给出正确答案)
[主观题]
在容积为3.0L的密闭容器中,装有CO2和H2混合物,存在下列可逆反应: 如果在此密闭容器中混合1.5mol CO2和4.
在容积为3.0L的密闭容器中,装有CO2和H2混合物,存在下列可逆反应:

如果在此密闭容器中混合1.5mol CO2和4.5mol H2,并加热到1123K时,反应达到平衡(已知此时Kc=1.0),计算:
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
在容积为3.0L的密闭容器中,装有CO2和H2混合物,存在下列可逆反应:

如果在此密闭容器中混合1.5mol CO2和4.5mol H2,并加热到1123K时,反应达到平衡(已知此时Kc=1.0),计算:
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在容积为3.0L的密闭容器中,装有CO2和H2混合物,存在下…”相关的问题
更多“在容积为3.0L的密闭容器中,装有CO2和H2混合物,存在下…”相关的问题
第1题
在容积为V=30×10-3m3的容器中,贮有温度为27℃,质量为2.2kg的CO2气体,
第2题
容器容积为20L,其中装有1.1kg的CO2气体,温度为13℃,试用范德瓦耳斯方程求气体的压强(取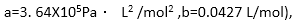 并与用理想气体状态方程求出的结果作比较。这时CO2气体的内压强多大?
并与用理想气体状态方程求出的结果作比较。这时CO2气体的内压强多大?
第3题
在容积为4×10-3m3的容器中,装有压强为5×102Pa的理想气体,则容器中气体分子的平均平移动能总和为().
A.2J
B.3J
C.5J
D.9J
第5题
g)和H2O(l)。过程放热401.727kJ。求
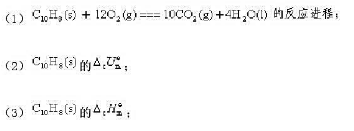
第7题
将装有0.1mol乙醚(C2H5)2O(l)的小玻璃瓶放入容积为10dm3的恒容密封真空容器中,并在35.51℃的恒温槽中恒温。35.51℃为在101.325kPa下乙醚的沸点。已知在此条件下乙醚的摩尔蒸发焓△vapHm=25.104kJ·mol-1。今将小瓶打破,乙醚蒸发至平衡态,求:(1)乙醚的蒸气压力;(2)过程的Q,△U,△H及△S。
第8题
热401.727kJ。求
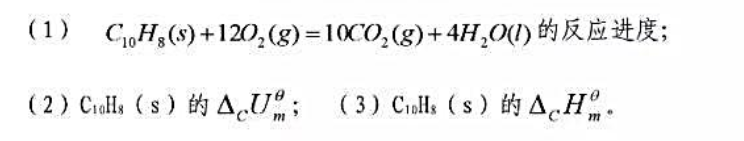
第10题
 。
。

为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧