25℃时,试计算: (1)25℃时CaCO3(s)在水中的溶解度; (2)25℃时CaCO3(s)在液中的溶解度。
25℃时,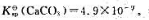 试计算:
试计算:
(1)25℃时CaCO3(s)在水中的溶解度;
(2)25℃时CaCO3(s)在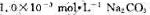 液中的溶解度。
液中的溶解度。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
25℃时,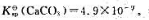 试计算:
试计算:
(1)25℃时CaCO3(s)在水中的溶解度;
(2)25℃时CaCO3(s)在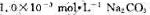 液中的溶解度。
液中的溶解度。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“25℃时,试计算: (1)25℃时CaCO3(s)在水中的溶…”相关的问题
更多“25℃时,试计算: (1)25℃时CaCO3(s)在水中的溶…”相关的问题
第1题
25℃时碘酸钡[Ba(IO3)2]在纯水中的溶解度为5.46×10-4mol·dm-3。假定可以应用德拜-休克尔极限公式,试计算该盐在0.01mol·dm-3CaCl2溶液中的溶解度。
第2题
在25℃时,电池:
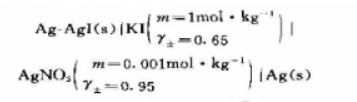
的电动势E=0.720V.试求:(1)AgI的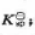 (2)AgI在纯水中的溶解度;(3)AgI在1mol·kg-1KI溶液中的溶解度.
(2)AgI在纯水中的溶解度;(3)AgI在1mol·kg-1KI溶液中的溶解度.
第3题
第4题
25℃时, 则25℃时AgSCN(s)在水中的溶解度s1=();在0.010mol·L-1AgNO3溶液中的溶解度s2=().
则25℃时AgSCN(s)在水中的溶解度s1=();在0.010mol·L-1AgNO3溶液中的溶解度s2=().
第5题
已知0℃,101.325kPa时,O2在水中的溶解度为4.49cm3/100g;N2在水中的溶解度为2.35cm3/100g。试计算被101.325kPa,体积分数ψ(N2)=79%,ψ(O2)=21%的空气所饱和了的水的凝固点较纯水的降低了多少?
第6题
在25℃时,求(1)AgCl在纯水中的溶解度;(2)AgCl在0.01mol·dm-3的KCl溶液中的溶解度。
第7题
25℃时、
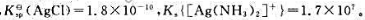 试计算25℃时在100mL10mol·L-1NH3溶液中能溶解AgCl固体的质量。
试计算25℃时在100mL10mol·L-1NH3溶液中能溶解AgCl固体的质量。
第9题
298.15K时,Mg(OH)2的标准溶度积常数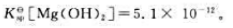 试计算:
试计算:
(1)Mg(OH)2在水中的溶解度:
(2)Mg(OH)2饱和溶液中的Mg2+、OH-的浓度和溶液的pH;
(3)Mg(OH)2在0.010mol·L-1NaOH溶液中的溶解度;
(4)Mg(OH)2在0.010mol·L-1MgCl2溶液中的溶解度。
第10题
计算25℃时,Ag2CrO4在0.001mol.L—1AgNO3溶液中的溶解度(用mol.L—1表示)。[已知KspΘ)(Ag2CrO4)=1.1×10—12]
第11题
25℃时,Cu元素在酸性溶液中的元素标准电极电势图为
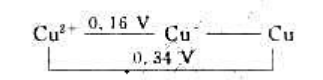
(1)试计算25℃时电对Cu2+/Cu的标准电极电势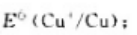
(2)已知2.303RT/F=0.060V,试计算25℃时Cu2+的歧化反应的标准平衡常数,


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧