题目内容
(请给出正确答案)
[主观题]
在T,V恒定条件下,反应A→产物为零级反应。反应物A的初始浓度cA,0=1mol,dm-3。t=0时的反应初速率vA,0=0.001mol,dm-3,s-1。计算反应的速率系数kA、半衰期t1/2及反应到cA=0.1mol,dm-3时所需的时间t各为若干?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在T,V恒定条件下,反应A→产物为零级反应。反应物A的初始浓…”相关的问题
更多“在T,V恒定条件下,反应A→产物为零级反应。反应物A的初始浓…”相关的问题
第1题
2mol·dm-3时,反应的初始速率为-(deA/dt)t=o=5x10-2mol·dm-1·s-1,求速率常数kA及kD.
第2题
第3题
28. 反应A+2B→D的速率方程为-dcA/dt=kcAcB,25℃时K=2×10-4dm3·mol-1·s-1。(1)若初始浓度cA,0=0.02mol·dm-3,cB,0=0.04mol·dm-3,求t1/2?(2)若将反应物A与B的挥发性固体装入5dm3的密闭容器中,已知25℃时A,B的饱和蒸气压分别为10kPa和2kPa,问25℃时0.5mol的A转化为产物需要多长时间?
第4题
第5题
第6题
第7题
某反应物A能够同时转化成三种不同的产物F、G、H,可表示为:
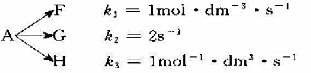
反应物初始浓度CA.0=2mo·dm8,设G为主产物,F和H为副产物,反应在等容密闭条件下进行.
(1)反应物浓度CA降到何值时,在何时生成的产物中主产物G的分数φ(CA)达到最大值?其最大值为多少?,
(2)反应终了时,cA=0,此时反应系统中G的浓度cG为多少?
第8题
在473K时,有反应A+2B→2C+D,其速率方程可写成r=k[A]x[B]y。实验(1):当A、B的初始浓度分别为[A]0=0.01mol·dm-3和[B]0=0.02mol·dm-3时,测得反应物B在不同时刻的浓度数据如下:
| t/h | 0 | 90 | 217 |
| [B]/(mol·dm-3) | 0.020 | 0.010 | 0.0050 |

第9题
零级反应A→P的半衰期t1/2与反应物A的初始浓度cA,0及反应速率常数kA的关系是t1/2=______。
第11题
A.零级反应
B.1.5级反应
C.2级反应
D.1级反应


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧