已知下列反应的值:试计算用H2还原和时的及.
已知下列反应的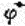 值:
值:
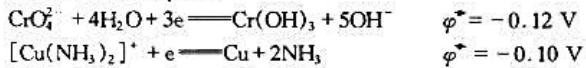
试计算用H2还原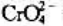 和
和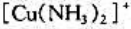 时的及
时的及 .
.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
已知下列反应的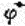 值:
值:
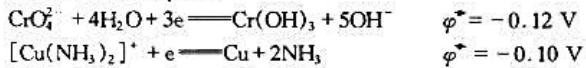
试计算用H2还原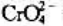 和
和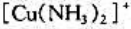 时的及
时的及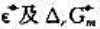 .
.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知下列反应的值:试计算用H2还原和时的及.”相关的问题
更多“已知下列反应的值:试计算用H2还原和时的及.”相关的问题
第1题
在相同控制条件下,用CO和H2还原同一种矿石,()表现的活化能值略大于();而用于还原不同的矿石时,活化能值有较大差别,这可能是反应处于不同的控制条件所致。
第2题
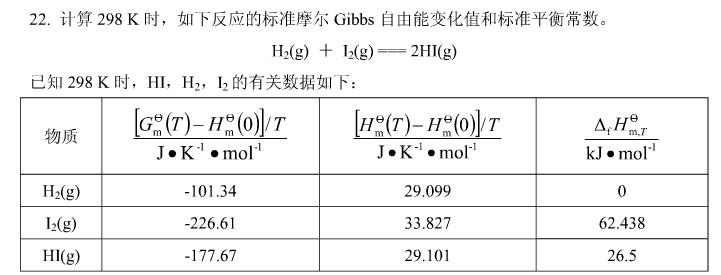
计算298K时,如下反应的标准摩尔Gibbs自由能变化值和标准平衡常数。
H2(g)+I2(g)====2HI(g)
已知298K时,HI、H2、I2的有关数据如下:
第3题
(1)在1393K下用H2还原FeO(s),平衡时混合气体中H2的摩尔分数为0.54。求FeO(s)的分解压。已知同温度下反应2H2O(g)====2H2(g)+O2(g)的Kθ=3.4×10-13;
(2)在炼铁中,FeO按如下反应还原:FeO(s)+CO(g)====Fe(s)+CO2(g)。计算1393K下还原1molFeO(s)需要CO若干摩尔。已知同温度下反应2CO2(g)====2CO(g)+O2(g)的Kθ=1.4×10-12。
第4题
已知反应:

298K时的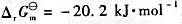 。试计算:
。试计算:
(1)该反应的标准平衡常数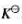 ;
;
(2)若空气中H2S的分压为3.1Pa,试计算可以确保铜单质免遭H2S腐蚀时H2的分压。
第5题
已知反应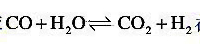 在700K时的平衡常数Kp=9,反应开始时系统中含有H2O、CO2、H2各1kmol,试求平衡组成.
在700K时的平衡常数Kp=9,反应开始时系统中含有H2O、CO2、H2各1kmol,试求平衡组成.
第6题
H2(g)和I2(g)在781K时发生如下反应:H2(g)+I2(g)→2HI(g)。已知HI的速率常数kHI为80.2dm3·mol-1·min-1,试求H2的速率常数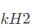 。
。
第7题
已知反应(CH3)2CHOH(g)===(CH3)2CO(g)+H2(g)在457K时的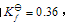 ,在298K时的
,在298K时的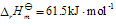 。(1)写出
。(1)写出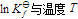 的函数关系式;(2)计算500K时的
的函数关系式;(2)计算500K时的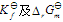 值。
值。
第8题
已知在定温(298K)、定压(101325pa)下,

试确定下列反应的热效应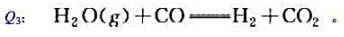 并计算该反应在2000K时的热效应.
并计算该反应在2000K时的热效应.
第9题
298K时,已知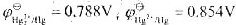 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
第11题
已知电对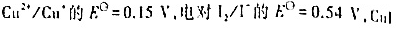 的
的
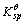 =1.3×10-12。
=1.3×10-12。
(1)试求氧化还原反应
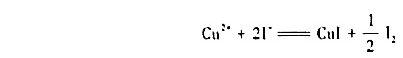
298K时的平衡常数;
(2)若溶液中Cu2+的起始浓度为0.10 mol·dm-3,I-的起始浓度为1.0 mol·dm-3,试计算达到平街时留在溶液中Cu2+的浓度。


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧