题目内容
(请给出正确答案)
[主观题]
在容积为40.0L氧气钢瓶中充有8.00kg的氧,温度为25℃.(1)按理想气体状态方程式计算钢瓶中氧的压力;(2)再根据vanderWaals方程计算氧的压力;(3)确定两者的相对偏差.
在容积为40.0L氧气钢瓶中充有8.00kg的氧,温度为25℃.(1)按理想气体状态方程式计算钢瓶中氧的压力;(2)再根据vanderWaals方程计算氧的压力;(3)确定两者的相对偏差.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在容积为40.0L氧气钢瓶中充有8.00kg的氧,温度为25…”相关的问题
更多“在容积为40.0L氧气钢瓶中充有8.00kg的氧,温度为25…”相关的问题
第2题
A.氧弹中氧气压力
B.钢瓶中氧气压力
C.p3
D.实验室大气压力
第3题
在273K时,1mol N2(g)的体积为7.03×10-5m3,试用下述几种方法计算其压力,并比较所得数值的大小。(1)用理想气体状态方程式;(2)用van der Waals气体状态方程式。
第6题
373K时,1.0kgCO2(g)的压力为5.07×103kPa,试用下述两种方法计算其体积。(1)用理想气体状态方程式;(2)用压缩因子图。
第7题
一个容积为0.5m3的钢瓶内,放有16kg温度为500K的CH4(g),试计算容器内的压力。(1)用理想气体状态方程;(2)由van der Waals方程。已知CH4(g)的常数a=0.228Pa·m6·mol-2,b=0.427×10-4m3·mol-1,M(CH4)=16.0g·mol。
第8题
A.300kPa
B.200kPa
C.150kPa
D.100kPa
第10题
1mol单原子理想气体,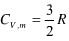 ,始态①的温度为273K,体积为22.4dm3,经历如下三步,又回到始态,请计算每个状态的压力、Q、W和△U。
,始态①的温度为273K,体积为22.4dm3,经历如下三步,又回到始态,请计算每个状态的压力、Q、W和△U。
(1)等容可逆升温由始态①到546K的状态②;
(2)等温(546K)可逆膨胀由状态②到44.8dm3的状态③;
(3)经等压过程由状态③回到始态①。
第11题
A、钢瓶内存有环氧丙烷
B、管理混乱
C、违章操作


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧