对于可逆反应N2+3H22NH3+Q下列说法正确的是()
A.达平衡时反应物和生成物的浓度都相等
B.达平衡后加入N2,当重新达到平衡时,NH3的平衡浓度比原平衡时增大,H2的浓度比原平衡时减少(反应前后体积不变)
C.达到平衡时,升高温度,加快了吸热反应速率,降低了放热反应速率,所以平衡向逆反应方向移动
D.达平衡后加入N2,当重新达到平衡时,N2在混合气中体积分数不变
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
A.达平衡时反应物和生成物的浓度都相等
B.达平衡后加入N2,当重新达到平衡时,NH3的平衡浓度比原平衡时增大,H2的浓度比原平衡时减少(反应前后体积不变)
C.达到平衡时,升高温度,加快了吸热反应速率,降低了放热反应速率,所以平衡向逆反应方向移动
D.达平衡后加入N2,当重新达到平衡时,N2在混合气中体积分数不变
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“对于可逆反应N2+3H22NH3+Q下列说法正确的是()”相关的问题
更多“对于可逆反应N2+3H22NH3+Q下列说法正确的是()”相关的问题
第1题
对于天然气水蒸气转化反应,下列说法正确的为()
A水蒸气转化反应是吸热的可逆反应
B低温对转化反应平衡有利
C高压有利于转化反应平衡
D低水碳比有利于转化反应
第2题
A.不同的可逆反应,反应物的性质不同,平衡常数是相同的
B.对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值就越大
C.对于同一个可逆反应,在不同温度下,平衡常数有相同的数值
D.对可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大
第3题
对于可逆反应
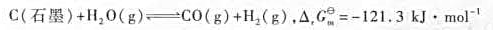 下列说法你认为是否正确?
下列说法你认为是否正确?
(1)达到平衡时各反应物和生成物的浓度相等;
(2)达到平衡时各反应物和生成物的浓度不再随时间的变化而改变;
(3)加入催化剂可以缩短反应达到平衡的时间;
(4)增加压强对平衡无影响;
(5)升高温度,平衡向右移动。
第4题
A.达平衡时反应物和生成物的浓度不发生变化
B.达平衡时正反应速率等于逆反应速率
C.达平衡时反应物和生成物的分压相等
D.达平衡时反应自然停止
第5题
A、不同的可逆反应,反应物的性质不同,平衡常数是相同的
B、对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大
C、对于同一个可逆反应,在不同温度下,平衡常数有相同的数值
D、对可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大
第6题
A.平衡组成与达到平衡的途径有关
B.r=r=0
C.升高温度,平衡不移动
D.反应物和生成物的分压不再发生改变
第7题
对于可逆反应:
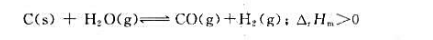
下列说法是否正确?为什么?
(1)达到化学平衡时各反应物和生成物的分压一定相等;
(2)改变生成物的分压,使
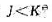 ,化学平衡向右移动;
,化学平衡向右移动;
(3)升高温度使正反应速率增大,逆反应速率减小,故化学平衡向右移动;
(4)由于反应前后分子数相等,所以增大压力对化学平衡没有影响;
(5)加入催化剂使正反应速率增大,化学平衡向右移动。
第8题
A.下列说法中可以充分说明这一反应已经达到化学平衡状态的是
B.SO2、O2、SO3的浓度比为2:1:2
C.SO2、O2、SO3在密闭容器中共存
D.SO2、O2、SO3的浓度不再发生变化
E.反应停止,正、逆反应速率都等于零
第9题
A.达平衡时p(H2O)=p(CO)=p(H2),即反应物与生成物压力相等
B.达平衡后p(H2O)、p(CO)、p(H2)不再改变
C.由于反应前后分子数不变,所以增加压力对平衡没有影响
D.升高温度,平衡逆向移动
第10题
A.恒温下,增大压力,由于产物分子数多,K值减小,平衡逆向移动
B.升高温度,反应速度加快,PCl的分解率增大
C.减小总压力,反应速度减慢,PCl转化率降低
D.降低温度,PCl的分解率降低,此反应为吸热反应
第11题
A.在同一条件下,对于一个可逆反应体系,当正反应速度大于逆反应速度时,此反应体系达到化学平衡
B.在同一条件下,对于一个可逆反应体系,当正反应速度小于逆反应速度时,此反应体系达到化学平衡
C.在同一条件下,对于一个可逆反应体系,当正反应速度等于逆反应速度时,此反应体系达到化学平衡


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧