已知反应CH3COOH(l)+C2H¿174175¿OH(l)=CH3COOC2H5(1)+H2O(1)的(
298K)=-9.20kJ·mol-1.25℃下,C2H¿174175¿OH(1)及CH3COOH(l)的标准燃烧焓分别为-1367kJ·mol-1和-875kJ·mol-1,CO2(g)和H2O(1)的标准生成焰分别为-394kJ·mol-1'和-286kJ·mol-1,计算25℃下CH3COOC2H5(1)的标准摩尔生成焓.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
298K)=-9.20kJ·mol-1.25℃下,C2H¿174175¿OH(1)及CH3COOH(l)的标准燃烧焓分别为-1367kJ·mol-1和-875kJ·mol-1,CO2(g)和H2O(1)的标准生成焰分别为-394kJ·mol-1'和-286kJ·mol-1,计算25℃下CH3COOC2H5(1)的标准摩尔生成焓.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知反应CH3COOH(l)+C2H¿174175¿OH(l…”相关的问题
更多“已知反应CH3COOH(l)+C2H¿174175¿OH(l…”相关的问题
第2题
已知下列电极反应的标准电极电势:
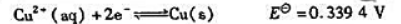
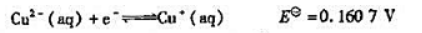
(1)计算反应: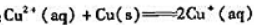 的KΘ;
的KΘ;
(2)已知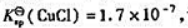 计算反应:
计算反应:
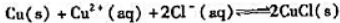 的标准平衡常数KΘ:
的标准平衡常数KΘ:
第7题
已知298.15K时,电极反应: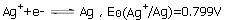 ,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e-
,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e- 2Ag+C2O2-4的标准电极电势
2Ag+C2O2-4的标准电极电势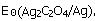 。
。
第8题
已知电极反应 (Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应
(Ag+/Ag)=0.7991V,Ag2C2O4的溶度积为3.4×10-11,计算电极反应 的标准电极电势
的标准电极电势(Ag2C2O4/Ag)。
第9题
已知反应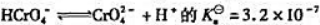 反应
反应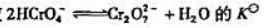 =33.
=33.
(1)计算反应 的标准平衡常数Kθ;
的标准平衡常数Kθ;
(2)计算1.0mol·L-1K2CrO4溶液中CrO42-与Cr2O72-浓度相等时溶液的pH.
第10题
已知下列标准电极电势
Cu2++2e-===Cu EΘ=0.337V
Cu2++e-===Cu+EΘ=0.153V
(1)计算反应Cu+Cu2+===2Cu+的平衡常数。
(2)已知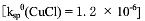 ,试计算下面反应的平衡常数。
,试计算下面反应的平衡常数。
Cu+Cu2++2Cl=2CuCl↓
第11题
已知反应2NO+O2====2NO2为三级反应。下列操作会使反应速率常数改变的是
(A) 减小体系的压力; (B) 在反应体系中加入大量的NO;
(C) 降低反应温度; (D) 在反应体系中加入NO2。


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧