题目内容
(请给出正确答案)
[主观题]
求在Fe电极上自1.00mol·dm-3KOH溶液中,每小时电解出1.00X10-4kg·cm-2的H2时应维持的电极电势.已知298K下,H2在铁电极上析出超电势的塔菲尔公式η=a+blg(J/[J])中a=0.76V,b=0.11V.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“求在Fe电极上自1.00mol·dm-3KOH溶液中,每小时…”相关的问题
更多“求在Fe电极上自1.00mol·dm-3KOH溶液中,每小时…”相关的问题
第2题
在电对Fe(OH)3/Fe(OH)2、Zn2+/Zn、
第3题
已知在1mol·L-1HC 1介质中,Fe(III)/Fe(II) 电对的Eθ=0.70V.
Sn(Ⅳ)/Sn(Ⅱ)电对的Eθ=0.14V.求在此条件下,反应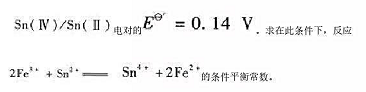 的条件平衡常数。
的条件平衡常数。
第4题
测定溶液pH值时,安装pH玻璃电极和饱和甘汞电极要求()
A、饱和甘汞电极端部略高于pH玻璃电极端部
B、饱和甘汞电极端部略低于pH玻璃电极端部
C、两端电极端部一样高
第5题
下述电池中的溶液当pH=9.18时,测得的电动势为+0.418;若换另一个未知溶液测得电动势为+0.312,计算298.15K时未知溶液的pH值。
(—)Pt|H2(100kPa)|H+(x mol·L-1)||饱和甘汞电极()
第9题

 ,试计算在c(H+)=1.0mol/L,c(
,试计算在c(H+)=1.0mol/L,c(


第10题
成年男性,电击伤28%,均为三度。休克期每小时尿量应维持
A.30ml
B.50ml
C.60ml
D.80ml
E.100ml
第11题
测定PH=10-13的碱性溶液时,应使用()作为指示电极。
A.231型玻璃电极
B.221型玻璃电极
C.普通型玻璃电极
D.甘汞电极


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧