试预测钫(Fr)元素的某些性质:(1)单质熔点很______;(2)其氯化物的晶格类型是______;(3)在空气中加热所得到的氧化物属于______;(4)电极电势很______;(5)其氢氧化物的碱性______。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“试预测钫(Fr)元素的某些性质:(1)单质熔点很______…”相关的问题
更多“试预测钫(Fr)元素的某些性质:(1)单质熔点很______…”相关的问题
第1题
试推断119号元素在元素周期表中的位置,并预言其下列性质:
①单质与水的反应;
②单质在氧气中燃烧的产物;
③比较它的溴化物和碘化物的热力学稳定性;
④预测它的碘化物的晶体类型;
⑤难溶化合物举例。
第2题
已知第四周期某些元素氯化物的熔点和沸点,试解释下列问题:
(1)KCl的熔点和沸点比(CaCl2低;
(2)CaCl2的熔点和沸点比FeCl2高,也比GeCl4高;
(3)FeCl2的熔点和沸点比ZnCl2高;
(4)FeCl2的熔点和沸点比FeCl3高;
(5)CaCl2的熔点和沸点比ZnCl2高;
已知相关数据如下表
氯化物 | KCl | CaCl2 | FeCl2 | ZnCl2 | FeCl3 | GeCl4 |
熔点/K | 1043 | 1055 | 945 | 488 | 555 | 223.5 |
沸点/K | 1773 | >1873 | 1303 | 1029 | 588 | 359.5 |
阳离子半径/pm | 133 | 99 | 76 | 74 | 64 | 53 |
第3题
试解释下列现象:
(1)碳与硅为同族元素,但其氧化物CO2,SiO2性质上相差极大.
(2)NaCl与AgCl化合物中阳离子都为+1,但AgCl难溶于水,NaCl易溶于水.
(3)第三周期元素氟化物熔点从SiF4开始突然下降:NaF(980℃),MgF2(1400℃),AlF3(1040℃),SiF4(-77℃),PF5(-83℃),SF6(-55℃).
(4)BeO熔点高于LiF,而FeCl3熔点又低于FeCl2.
(5)HgS,CdS,ZnS颜色差异.
第4题
| (14分)下表所示的是第二周期元素中,除Be、B、Ne三种元素外,其它元素的简单氢化物的沸点;题26图所示是第三周期元素中,除Ar以外的其它元素的单质的熔点变化关系。
(1)X的简单氢化物属于____分子(填“极性”或“非极性”),G元素的单质在固态时的晶体类型为________。 (2)写出W的氢化物的电子式__________。 (3)A和Z两元素形成的一种化合物分子中各原子最外均达到8电子稳定结构,则该分子的结构式为____。 (4)化合物AY能与水反应生成两种弱酸,其化学方程式为____ (5)写出元素F的单质与三氧化二铬反应的化学方程式_______ |
第5题
一般单质在空气中的燃烧产物为该元素的____。
A.氧化物
B.化合物
C.还原物
D.以上都不是
第6题
试判断下列各种物质各属何种晶体类型,并写出熔点从高到低的顺序。
(1)KCl (2)SiC (3)HI (4)BaO
第7题
A.Li 2 SO 4 难溶于水
B.Li与冷水剧烈反应
C.LiOH是易溶于水,受热不分解的强碱
D.Li 2 CO 3 受热分解,生成Li 2 O和CO 2
第8题
第9题
第10题
第11题
下表列山了前20号元素中的某些元素性质的有关数据。
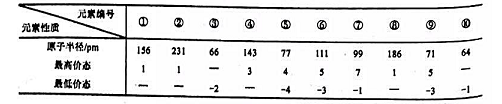
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是()(填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)()。某元素R的原子半径为1.04x10-10m,该元素最高价氧化物的水化物化学式为()。


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧