右下表列出HI分解反应(2HI=H2(g)+I2(g))在不同温度下的反应速率,试用两种方法确定该反应的活化能.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“右下表列出HI分解反应(2HI=H2(g)+I2(g))在不…”相关的问题
更多“右下表列出HI分解反应(2HI=H2(g)+I2(g))在不…”相关的问题
第1题
在不同温度下,测定H2+I2→2HI的反应速率常数如下表所示:
 试用作图法求反应活化能,并求在300℃和400℃的速率常数各是多少?
试用作图法求反应活化能,并求在300℃和400℃的速率常数各是多少?
第2题
在不同温度下测得的某污染物催化分解反应的速率常数k如下表所示,求出反应的活化能和频率因子。
| 温度/K | 413.2 | 433.2 | 453.2 | 473.2 | 493.2 |
| k/(mol·g-1·h-1) | 2.0 | 4.8 | 6.9 | 13.8 | 25.8 |
第3题
有关反应速率的叙述中错误的是()。
A.绝大多数反应的反应速率随温度升高而增大
B.活化能大的反应速率也大
C.速率常数大的反应速率大
D.对于相同温度下的不同的反应,活化能越大,速率常数随温度的变化率越大
第4题
半水合磷酸铡晶体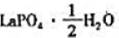 受热时将失去结晶水,而得到无水磷酸镧
受热时将失去结晶水,而得到无水磷酸镧
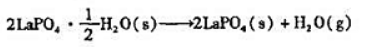
在不同温度下该反应速率常数如表3—4.

用不同的方法计算该反应的活化能.
第5题
HI(g)的分解反应在836K时其速率常数k=0.00105s-1,在943K时的速率常数k=0.00268s-1。试计算:
(1)该反应的活化能Ea;
(2)在773K时的速率常数k。
第6题
在相同温度下,三个基元反应的活化能如下:
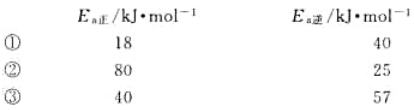
A.正向反应速率最大是()反应。
B.第一个反应的热效应为()kJ·mol-1。
C.逆反应为放热反应的是()反应。
第7题
反应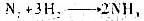 ,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
第8题
在不加催化剂时,H2O2的分解反应的活化能为75.00kJ·mol-1。当以铁为催化剂时,该反应的活化能降到54.00kJ·mol-1。试计算在25℃时,此两种条件下,该反应速率的比值。
第9题
在没有催化剂存在时,H2O2的分解反应: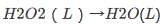
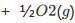 活化能为75kJ·mol-1。当有铁催化剂存在时,该反应的活化能就降低到54kJ·mol-1。计算在298K时此两种反应速率的比值。
活化能为75kJ·mol-1。当有铁催化剂存在时,该反应的活化能就降低到54kJ·mol-1。计算在298K时此两种反应速率的比值。
第10题


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧