计算下述催化加氢反应,在298K和标准压力下的熵变。已知C2H2(g)、H2(g)、C2H5(g)在298 K时的标
计算下述催化加氢反应,在298K和标准压力下的熵变。
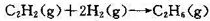
已知C2H2(g)、H2(g)、C2H5(g)在298 K时的标准摩尔熵分别为200.8J·mo1-1·K-1,130.6J·mol-1·K-1和229.5J·mol-1·K-1。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
计算下述催化加氢反应,在298K和标准压力下的熵变。
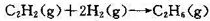
已知C2H2(g)、H2(g)、C2H5(g)在298 K时的标准摩尔熵分别为200.8J·mo1-1·K-1,130.6J·mol-1·K-1和229.5J·mol-1·K-1。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“计算下述催化加氢反应,在298K和标准压力下的熵变。已知C2…”相关的问题
更多“计算下述催化加氢反应,在298K和标准压力下的熵变。已知C2…”相关的问题
第2题
已知下列反应在298K时的标准摩尔焓变:
已知下列反应在298k时的标准摩尔焓变
(1) 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g)
(2) 2H2(g)+O2(g)=2H2O(l)
(3) C(石墨)+O2(g)=CO2(g)
(4) H2O(g)=H20(l)
根据以上数据 计算DfHmy(C2h2.g 298k )
第4题
已知在定温(298K)、定压(101325pa)下,

试确定下列反应的热效应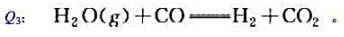 并计算该反应在2000K时的热效应.
并计算该反应在2000K时的热效应.
第5题
第6题
已知反应:
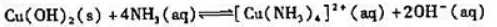
(1)计算该反应在298K下的标准平衡常数;
(2)估算Cu(OH)2在6.0mol·L-1氨水中的溶解度(mol·L-1)(忽略氨水浓度的变化).
第7题
反应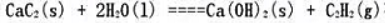 在298K下的标准摩尔热力学能变化量为-128kJ.mol-1。求该反应的标准摩尔焓变。
在298K下的标准摩尔热力学能变化量为-128kJ.mol-1。求该反应的标准摩尔焓变。
第8题
已知反应2H2O2====2H2O+O2的活化能Ea为71kJ·mol-1,在过氧化氢酶的催化下,活化能降至8.4kJ·mol-1。试计算298K时在酶催化下,H2O2分解速率为原来的多少倍?
第9题
(1)计算298K下反应: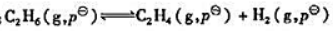 的
的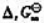 并判断在标准状态下反应向何方进行.
并判断在标准状态下反应向何方进行.
(2)计算298K反应: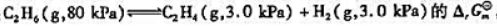 并判断反应方向.
并判断反应方向.


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧