对于CO2气体有范德瓦耳斯常量0°C时其摩尔体积为6.0x10-4m3·mol-1。试求
对于CO2气体有范德瓦耳斯常量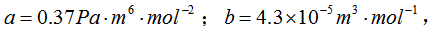 0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
对于CO2气体有范德瓦耳斯常量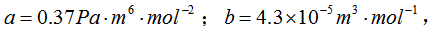 0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“对于CO2气体有范德瓦耳斯常量0°C时其摩尔体积为6.0x1…”相关的问题
更多“对于CO2气体有范德瓦耳斯常量0°C时其摩尔体积为6.0x1…”相关的问题
第3题
第4题
把氧气当作范德瓦耳斯气体,它的范德瓦耳斯方程常量为a=1.36×10-1m6·Pa·mol-2,b=32×10-6m3·mol-1.试问压强为10.1MPa,密度为100kg·m-3的氧气的温度是多少?并把结果与氧气当作理想气体时的结果作比较.
第5题
范德瓦尔气体向真空自由膨胀,其体积增加一倍,若气体的初态为T1、υ1,比热容cv为常数,试求气体的熵变。
第6题
CO2气体在40℃时的摩尔体积为0.381dm3·mol-1。设CO2为范德华气体,试求其压力,并比较与实验值5066.3kPa的相对误差。
第7题
12. CO2气体在40℃时的摩尔体积为0.381dm3·mol-1。设CO2为范德华气体,试求其压力,并比较与实验值5066.3kPa的相对误差。
第9题
导出遵守范德瓦尔状态方程的气体的cp-cv表达式,并证明满足范德瓦尔方程的气体比定容热容不随气体比体积变化。
第11题
1mol范德瓦尔斯气体,初始体积为V1,向真空作绝热膨胀至体积为V2.(1)求温度的增量△T;(2)气体温度的变化是否由于其内能变化了?(3)如果这是理想气体,温度变化如何?


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧