题目内容
(请给出正确答案)
[主观题]
二级反应2A→B的活化能为85.0kJ·mol-1.35℃下用A进行反应,初浓度为0.500mol·dm-3,测得半衰期为4.50min.计算50℃下,用初浓度为0.500mol·dm-3的A进行同样的反应,半衰期为何?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“二级反应2A→B的活化能为85.0kJ·mol-1.35℃下…”相关的问题
更多“二级反应2A→B的活化能为85.0kJ·mol-1.35℃下…”相关的问题
第1题
二级反应A+D→G的活化能为92.05kJ/mol。A和D的初浓度均为1mol/L,在293.15K30分钟后,两者各消耗一半。
求:
(1)在293.15K1小时后两者各剩多少;
(2)313.15K温度下的速率常数。
第3题
A、若为二级反应,则必为双分子反应
B、若为双分子反应,则必为二级反应
C、若为二级反应,则必为基元反应
D、若为二级反应,则必为复杂反应
第5题
实验测得乙醛(CH3CHO)的热分解活化能为200.8kJ·mol-1,速率方程为:
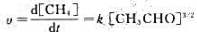
有人提出该分解反应机理为:
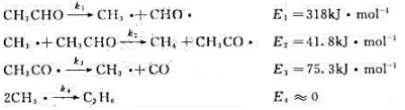
试推断上述反应机理是否合理,并求该反应的活化能.
第6题
65℃时进行反应N2O5(g)=N2O4(g)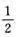 +O2(g),测得N2O5的分解速率常数为0.292min-1,反应的活化能为103kJ·mol-1,计算15℃时此反应的k及t1/2.
+O2(g),测得N2O5的分解速率常数为0.292min-1,反应的活化能为103kJ·mol-1,计算15℃时此反应的k及t1/2.
第7题
第8题
反应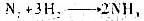 ,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
第9题
反应:
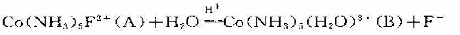
被酸催化.若反应速率公式为:

在一定温度及初始浓度条件下测得分数衰期如下:
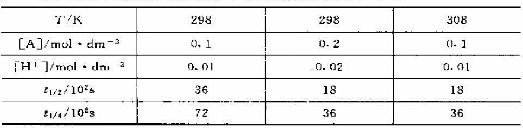
其中t1/4是指当反应物浓度为起始浓度的1/4时所需时间.求:
(1)反应级数a和β的数值;
(2)不同温度时的反应速率常数k值;
(3)反应实验活化能Ea值.
第10题
反应A-Y+Z是吸热反应,正反应的活化能为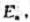 逆反应的活化能为
逆反应的活化能为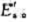 则正反应的活化能与逆反应的活化能之间的关系为()。
则正反应的活化能与逆反应的活化能之间的关系为()。
A、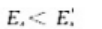
B、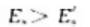
C、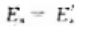
D、三种都有可能
第11题


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧