298K时,电池的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.(1)写出电池反应;(2
298K时,电池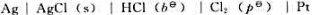 的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
(1)写出电池反应;
(2)计算298K时该反应的 和标准平衡常数
和标准平衡常数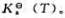
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
298K时,电池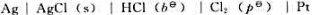 的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
(1)写出电池反应;
(2)计算298K时该反应的 和标准平衡常数
和标准平衡常数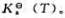
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“298K时,电池的电动势为1.1362v,电动势的温度系数为…”相关的问题
更多“298K时,电池的电动势为1.1362v,电动势的温度系数为…”相关的问题
第1题
测得电池Zn(s)|ZnCl2(a=0.05)|AgCl(s)|Ag(s)的电动势在298K时为1.015V,温度系数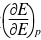 为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
第2题
298K时,下列电池的电动势为1.228V:
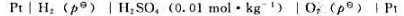
已知H2O(I)的标准生成焓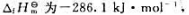 试求:
试求:
(1)该电池的温度系数:
(2)该电池在273K时的电动势.设反应焓在273~298K间为常数.
第3题
电池Pb|PbSO4(s)|Na2SO4·10H2O(饱和溶液)|Hg2SO4(s)|Hg在25℃时电动势为0.9647V,电动势的温度系数为1.74×10-4V·K-1。(1)写出电池反应;(2)计算25℃时该反应的△rGm,△rSm,△rHm及电池恒温可能放电时该反应过程的Qr,m。
第4题
t(s)的电动势E=-1.228V,H2O(l)的标准生成焰为-285.5kJ·mol-1,请:
(1)写出电极反应及电池反应;
(2)求该电池的电动势温度系数;
(3)求电池反应的 ;
;
(4)求273K时电池的电动势(假设反应热ΔtHmθ在0~25C之间不随温度变化).
第5题
在298K时,电池Hg(1)|Hg2Cl2(s)|HCl(a)|Cl2(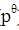 )|Pt(s)的电动势为1.092V,温度系数为9.427×10-4V·K-1。
)|Pt(s)的电动势为1.092V,温度系数为9.427×10-4V·K-1。
第6题
测得电池Zn|ZnCl2(a=0.05)|AgCl(s)|Ag的电动势在298.15K时为1.015V,温度系数TCR为-4.92×10-4V/K,试写出电池反应并计算当电池可逆放电2mol电子电量时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
第7题
有如下电池
Cu(s)|CuAc2(0.1mol·kg-1)|AgAc(s)|Ag(s)
已知298K时该电池的电动势E(298K)=0.372V,温度为308K时,E(308K)=0.374V,设电动势随温度的变化是均匀的。又已知298K时,
第8题
根据下列反应组成电池
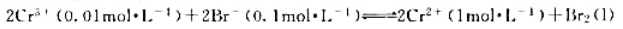
(1)写出电池符号;
(2)计算298K时的电动势,并判断反应自发进行的方向;
已知
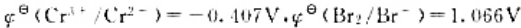
第9题
试为下述反应设计一电池
Cd(s)+I2(s)====Cd2+(a=1)+2I-(a=1)
求电池在298K时的标准电动势E、反应的△rG和平衡常数Kθ。
第10题
电池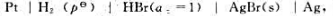 请:
请:
(1)写出电极反应与电池反应:
(2)若电池的电动势E/V=0.07131-4.99×10-6×(T/K-298),求正极在298K时的标准电极电势Eθ及电池反应的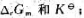
(3)判断此电池在298K时吸热还是放热,为什么?
(4)若HBr的浓度b=0.1mol·kg-1,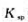 =1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
=1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
第11题
电池(Pt)H2(pθ)IH2SO4(0.01mol·kg-1)|O2(pθ)(Pt)在25℃时电动势E=1.228V,已知液态水的△rHmθ(298K)=-2.861×10J·mol-1.
(1)计算此电池电动势的温度系数;
(2)假定温度在0-25℃之间,此反应的△rHmθ为常数,计箅电池在0℃时的电动势.


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧