题目内容
(请给出正确答案)
[主观题]
有反应3C(s)+2H2</sub>O(g)=-CH4</sub>(g)+2CO(g),试讨论一定温度时,下列情况下平衡移动的方向,并简要说明理由.(1)采用压缩的方法使系统压力增大;(2)充人氮气但保持系统总体积不变;(3)充人氮气但保持系统总压力不变;(4)充人水蒸气但保持系统总压力不变;(5)向反应系统加炭并保持系统总压力不变.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“有反应3C(s)+2H2O(g)=-CH4(g)+2CO(g…”相关的问题
更多“有反应3C(s)+2H2O(g)=-CH4(g)+2CO(g…”相关的问题
第1题
第2题
可逆反应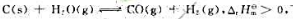 下列说法正确的是().
下列说法正确的是().
A、达到平衡时反应物和生成物的分压相等
B、降低温度有利平衡向正反应方向移动
C、升高温度有利于平衡向正反应方向移动
D、增大压力对平衡没有影响
第3题
在其它条件不变的情况下,升高温度会使反应平衡向()方向移动。
A.放热
B.吸热
C.既不吸热,也不放热
第4题
时,平衡向气体分子数()的方向移动。如气体反应前后分子数无变化时,则增加压力对平衡()。
第6题
可逆反应 达到平衡后,升高温度,平衡向正反应方向移动。这说明()
达到平衡后,升高温度,平衡向正反应方向移动。这说明()
A、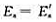
B、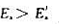
C、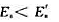
D、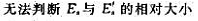
第7题
A.增加反应物浓度,使平衡向生成物方向移动
B.增加气体反应的总压力时,平衡向气体分子数减少的方面移动
C.升高温度会使化学平衡的吸热反应的方向移动
D.催化剂不影响化学平衡
第10题
根据平衡移动原理,讨论下列反应:
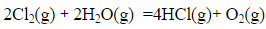
将Cl2、H2O、HCI、O2四种气体混合,反应达平衡时,若进行下列各项操作,对平衡数值各有何影响(操作项目中没有注明的是指温度不变、体积不变)?化学平衡如何移动?
操作项目 平衡数值 操作项目 平衡数值
(1)加O2H2O的物质的量 (5)减小容器的体积
(2)加O2O2的物质的量 (6)升高温度
(3)增大容器的体积 H2O的物质的量 (7)升高温度 HCl的分压
(4)减小容器的体积 Cl2的分压 (8)加催化剂 HCl的物质的量
第11题


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧