化学法制备的二氧化氯溶液浓度一般在()%左右
A.1
B.2
C.3
D.4
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
A.1
B.2
C.3
D.4
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“化学法制备的二氧化氯溶液浓度一般在()%左右”相关的问题
更多“化学法制备的二氧化氯溶液浓度一般在()%左右”相关的问题
第1题
【题目描述】
18.(10分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4===2ClO2↑+Na2SO4+O2↑+2H2O

用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是▲。
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子的含量应不超过0.2mg·L-1。
饮用水中CIO2、CIO2的含量可用连续碘量法进行测定。CIO2被I-还原为CIO-2、Cl-的转化率与溶液pH的关系如右图所示。当pH≤2.0时,CIO-2也能被I-完全还原成Cl-。反应生成的I2用标准Na2S2O3溶液滴定: ①请写出pH≤2.0时,CIO-2与I-反应的离子议程式▲。 ②请完成相应的实验步骤: 步骤1:准确量取V mL水样加入到锥形瓶中。 步骤2:调节水样的pH为7.0~8.0。 步骤3:加入足量的KI晶体。 步骤4:加少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。 步骤5:▲。 ③根据上述分析数据,测得该饮用水样中CIO-2的浓度为▲mol·L-1(用含字母的代数式表示。) ④若饮用水中ClO-2的含量超标,可向其中加入适量的Fe2+将ClO-2还原成Cl-, 该反应的氧化产物是▲(填化学式)。
(1)方法二制备的ClO2中不含Cl2

第2题
A.在标定和使用标准滴定溶液时,滴定速度一般应保持6-8mL/min
B.制备标准滴定溶液的浓度应该在规定浓度的±5%范围以内
C.标定运算过程中保留5位有效数字,最终标定报出结果为4位有效数字
D.配制好的硝酸银标准滴定溶液,不需避光保存
第3题
现有KNO3和NaNO2的混合样品5.000g,制备成500.0mL的溶液,移液25.00mL,用浓度为0.1200mol·L-1的Ce4+标准溶液50.00mL在强酸中氧化,过量的Ce4+用浓度为0.02500mol·L-1的Fe2+标准溶液滴定,用去Fe2+溶液28.40mL,相应的反应如下:
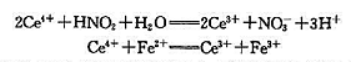
(1)若将第一个反应式作为原电池的电池反应写出该原电池的电极反应并计算该电池反应的ΔrGmθ[已知ϕθ(Ce4++/Ce3+)=1.44V,ϕθ(NO3-/NO2-)=0.934V]
(2)计算试样中NaNO2的质量分数w.[已知M(NaNO2)=69.00g.mol-1]
(3)计算第一步的标准平衡常数Kθ.
解题思路:注意原电池的写法.此题依然是考查电化与热力学、化学平衢间的计算.
第5题
A.在标定和使用标准滴定溶液时,滴定速度一般应保持在6mL/min-8mL/min
B.称量工作基准试剂的质量的数值小于等于0.5g时,按精确至0.01mg称量
C.制备标准滴定溶液的浓度值应在规定浓度值的士5%范围以内
D.除另有规定外,标准滴定溶液在常温(20℃)下保存时间一般不超过两个月
第6题
A.单凝聚法中调节明胶的pH至等电点即可使明胶产生胶凝而成囊
B.复凝聚法的制备原理是两种带相反电荷的复合囊材,在一定条件下两种囊材在溶液中正负电的结合而凝聚成囊
C.影响单凝聚法成囊的因素除凝聚系统外还与明胶溶液浓度及温度有关
D.在沉降囊中调节pH到8~9加37%甲醛溶液与15℃以下使囊固化
E.在单凝聚法中加入硫酸钠的作用是增加溶液的离子强度
第7题
A.单凝聚法中调节明胶的pH至等电点即可使明胶产生胶凝而成囊
B.复凝聚法的制备原理是两种带相反电荷的复合囊材,在一定条件下两种囊材在溶液中正负电的结合而凝聚成囊
C.影响单凝聚法成囊的因素除凝聚系统外还与明胶溶液浓度及温度有关
D.在沉降囊中调节pH到8~9,加37%甲醛溶液与15℃以下使囊固化
E.在单凝聚法中加入硫酸钠的作用是增加溶液的离子强度
第9题
A.甲凝聚法是相分离法常用的一种方法
B.在单凝聚法中加人硫酸钠主要是增加溶液的离子强度
C.成囊的影响因素除凝聚系统外还与明胶溶液浓度和温度有关
D.在沉降囊中调节pH8.0~9.0,加入37%甲醛溶液于15℃以下使微囊固化。
E.单凝聚法中调节pH至明胶等电点即可成囊


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧