下列说法正确的是()
A.25℃时,pH=12.0的KOH溶液中,由水电离出的(OH-)=10-12mol/L
B.25℃时,pH=12.0的KCN溶液中,由水电离出来的(OH-)=10-12mol/L
C.25℃时, 若某溶液水电离的氢离子浓度为10-5mol/L,则该溶液的pH为5
D.25℃时, 若某溶液水电离的氢离子浓度为10-11mol/L,则该溶液的pH为11
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
A.25℃时,pH=12.0的KOH溶液中,由水电离出的(OH-)=10-12mol/L
B.25℃时,pH=12.0的KCN溶液中,由水电离出来的(OH-)=10-12mol/L
C.25℃时, 若某溶液水电离的氢离子浓度为10-5mol/L,则该溶液的pH为5
D.25℃时, 若某溶液水电离的氢离子浓度为10-11mol/L,则该溶液的pH为11
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“下列说法正确的是()”相关的问题
更多“下列说法正确的是()”相关的问题
第1题
A.水的电离是放热过程
B.水的pH 值在25℃时大于在18℃时
C.在18℃时,水中氢氧根离子的浓度是0.8×10-7 mol /L
D.仅在25℃时,水才是中性的
第2题
水的质子自递反应,已知在18℃时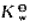 =6.4×10-15,25℃时
=6.4×10-15,25℃时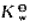 =1.0×10-14.
=1.0×10-14.
下列说法正确的是()。
A.水的质子自递反应是放热过程
B.水的质子自递反应是减反应
C.在18℃时,水的pH小于25℃时的pH
D.在18℃时,水中H+的浓度是8.0×10-8mol·L-1
第3题
A.水的电离是放热过程
B.在25℃ 时水的pH值大于在18℃ 时的pH
C.在18℃ 时,水中氢氧根离子的浓度是0.8 ´ 10-7 mol·dm-3
D.仅在25℃ 时,水才是中性的
第4题
A.1 mol月球背面的氦-3(3He)含有质子为2NA
B.标准状况下,22.4 L甲烷和1 mol Cl2反应后的混合物中含有氯原子数小于2NA
C.2 mol SO2与1 mol O2充分反应,转移的电子数为4NA
D.25 ℃时,1 L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2NA
第5题
A.25℃时,0.1molL-1HF 溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中没有沉淀产生
D.该体系中HF与CaCl2反应产生沉淀
E.该体系中HF与CaCl2不反应
第6题
25℃时测得某溶液pH为6.25,下列描述正确的是
A、溶液呈氧化性
B、溶液呈碱性
C、溶液呈中性
D、溶液呈还原性
E、溶液呈酸性
第7题
25℃时,测得某溶液pH为7.00,下列描述方法正确的是
A、溶液呈氧化性
B、溶液呈碱性
C、溶液呈中性
D、溶液呈还原性
E、溶液呈酸性
第8题
当下列电池中的溶液是pH=4.00的缓冲溶液时,在25℃测得电池的电动势为0.209V:玻璃电极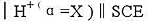 当缓冲溶液由未知溶液代替时,测得电池电动势如下:
当缓冲溶液由未知溶液代替时,测得电池电动势如下:
(a)0.312V; (b)0.088V; (c)-0.017V.试计算每种溶液的pH.
第9题
A.囊材浓度以25%~5%为宜
B.成囊时pH应调至4.0~4.5
C.成囊时温度应为50~55℃
D.甲醛固化时温度在10℃-15℃
E.甲醛固化时pH应调至8~9
第10题
![分别计算25℃时,pH=8.0和[H+]=5.0mol/L条件下,电对H3AsO4/HAsO2的条件](https://img2.soutiyun.com/ask/2020-11-16/974370598904697.jpg)
![分别计算25℃时,pH=8.0和[H+]=5.0mol/L条件下,电对H3AsO4/HAsO2的条件](https://img2.soutiyun.com/ask/2020-11-16/974370610828379.jpg) 并判断pH=8.0和[H+]=5.0mol/L条件下,下列反应的方向:
并判断pH=8.0和[H+]=5.0mol/L条件下,下列反应的方向:![分别计算25℃时,pH=8.0和[H+]=5.0mol/L条件下,电对H3AsO4/HAsO2的条件](https://img2.soutiyun.com/ask/2020-11-16/974370640959102.jpg) 。
。

为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧