在298K和标准压力时,电解含有Ag+(=0.05)、Fe2+(=0.01)、Cd2+(=0.001)、Ni2+(=0.1)和H+(=0.001)的混合溶液,并设
在298K和标准压力时,电解含有Ag+(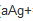 =0.05)、Fe2+(
=0.05)、Fe2+(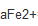 =0.01)、Cd2+(
=0.01)、Cd2+(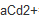 =0.001)、Ni2+(
=0.001)、Ni2+(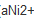 =0.1)和H+(
=0.1)和H+(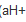 =0.001)的混合溶液,并设
=0.001)的混合溶液,并设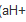 不随电解的进行而变化,又已知H2(g)在Ag、Ni、Fe和Cd上的超电势分别为0.20V、0.24V、0.18V和0.30V。当外加电压从零开始逐渐增加时,试用计算说明在阴极上析出物质的顺序。
不随电解的进行而变化,又已知H2(g)在Ag、Ni、Fe和Cd上的超电势分别为0.20V、0.24V、0.18V和0.30V。当外加电压从零开始逐渐增加时,试用计算说明在阴极上析出物质的顺序。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


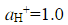 的水溶液,当所用的电流密度j=5×10-3A·cm-2时,计算使电解能顺利进行的最小分解电压。已知
的水溶液,当所用的电流密度j=5×10-3A·cm-2时,计算使电解能顺利进行的最小分解电压。已知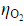 =0.487V,
=0.487V,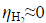 ,忽略电阻引起的电位降,H2O(l)的标准摩尔生成Gibbs自由能
,忽略电阻引起的电位降,H2O(l)的标准摩尔生成Gibbs自由能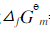 =-237.129kJ·mol-1。
=-237.129kJ·mol-1。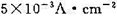 时,计算使电解能顺利进行的最小分解电压。已知
时,计算使电解能顺利进行的最小分解电压。已知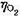 =0.487V,
=0.487V,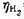 ≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能
≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能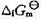 =-237.129kJ·mol-1.
=-237.129kJ·mol-1.


















