在298K和标准压力下,用镀铂黑的铂电极电解aH+=1.0的水溶液,当所用的电流密度j= 时,计算使电解
在298K和标准压力下,用镀铂黑的铂电极电解aH+=1.0的水溶液,当所用的电流密度j=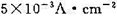 时,计算使电解能顺利进行的最小分解电压。已知
时,计算使电解能顺利进行的最小分解电压。已知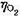 =0.487V,
=0.487V,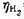 ≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能
≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能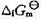 =-237.129kJ·mol-1.
=-237.129kJ·mol-1.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
在298K和标准压力下,用镀铂黑的铂电极电解aH+=1.0的水溶液,当所用的电流密度j=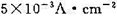 时,计算使电解能顺利进行的最小分解电压。已知
时,计算使电解能顺利进行的最小分解电压。已知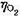 =0.487V,
=0.487V,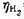 ≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能
≈0,忽略电阻引起的电位降,H2O(I)的标准摩尔生成Gibbs自由能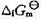 =-237.129kJ·mol-1.
=-237.129kJ·mol-1.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在298K和标准压力下,用镀铂黑的铂电极电解aH+=1.0的…”相关的问题
更多“在298K和标准压力下,用镀铂黑的铂电极电解aH+=1.0的…”相关的问题
第1题
在298K和标准压力下,用镀铂黑的铂电极电解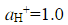 的水溶液,当所用的电流密度j=5×10-3A·cm-2时,计算使电解能顺利进行的最小分解电压。已知
的水溶液,当所用的电流密度j=5×10-3A·cm-2时,计算使电解能顺利进行的最小分解电压。已知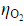 =0.487V,
=0.487V,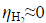 ,忽略电阻引起的电位降,H2O(l)的标准摩尔生成Gibbs自由能
,忽略电阻引起的电位降,H2O(l)的标准摩尔生成Gibbs自由能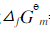 =-237.129kJ·mol-1。
=-237.129kJ·mol-1。
第2题
θ)|Pt
(1)写出电解时的电极反应及电解反应;
(2)计算298K时.在电流密度为50A·m-2条件下的分解电压.已知此时铂电极上的超电势:Eθ(OH,H2O|O2|Pt)=0.401V.η(H2)=0,η(O2)=0.487V;
(3)当所用的电流密度为50A·m-2时.计算使电解能顺利进行的最小分解电压.
已知ΔtGmθ(H2O,l)=-237.1kJ·mol-1.
第3题
25°C下用铂电极电解1mol.dm-3的H2SO4水溶液.
(1)计算理论分解电压;
(2)若两电极面积均为1cm2,电解液电阻为100Ω,H2(g)和O2(B)的超电势η与电流密度J的关系分别为

问当通过的电流为1mA时,外加电压为若干?
第4题
在298K和标准压力下,当电流密度为0.1A·cm-2时,H2(g)和O2(g)在Ag(s)电极上的超电势分别为0.87V和0.98V。今用Ag(s)电极电解浓度为0.01mol·kg-1的NaOH溶液,问这时在两个银电极上首先发生什么反应?此时外加电压为多少(设活度因子为1)?
第5题
在298K和标准压力下,以Pt为阴极,C(石墨)为阳极,电解含CdCl2(0.01mol·kg-1)和CuCl2(0.02mol·kg-1)的水溶液。若电解过程中超电势可忽略不计, (设活度因子均为1),试问:
(设活度因子均为1),试问:

第6题
25℃时用铂电极电解1mol·dm-3的H2SO4。(1)计算理论分解电压;(2)若两电极面积为1cm2,电解液电阻为100Ω,H2(g)和O2(g)的超电势η与电流密度J的关系分别为η(H2,g)/V=0.472+0.1181g[J/(A·cm-2)],η(O2,g)/V=1.062+0.118lg[J/(A·cm-2)],问当通过的电流为1mA时,外加电压为若干?
第7题
25℃时以铂为电极电解含有NiCl2(0.01mol·dm-3)和CuCl2(0.02mol·dm-3)的水溶液。若电解过程中超电势可忽略,问:
第8题
在298K和标准压力下,用铁Fe(s)为阴极,C(石墨)为阳极,电解6.0mol·kg-1的NaCl水溶液。若H2(g)在铁阴极上的超电势为0.20V,O2(g)在石墨阳极上的超电势为0.60V,Cl2(g)的超电势可忽略不计,试说明两极上首先发生的反应及计算至少需加多少外加电压,电解才能进行(设活度因子均为1)。
第11题
298K时,用Pb(s)为电极来电解H2SO4溶液,已知其浓度为0.10mol·kg-1,γ±=0.265,若在电解过程中,把Pb阴极与另一甘汞电极相连组成原电池,测得其电动势E=1.0685V。试求H2(g)在Pb阴极上的超电势(只考虑H2SO4的一级解离)。已知所用甘汞电极的电极电势φ甘汞=0.2806V。


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧