在448~688K的温度区间内,用分光光度法研究了下面的气柑反应:I2+环戊烯2HI+环戊二烯,得到K
在448~688K的温度区间内,用分光光度法研究了下面的气柑反应:
I2+环戊烯 2HI+环戊二烯,得到KƟp与温度(K)的关系为:
2HI+环戊二烯,得到KƟp与温度(K)的关系为: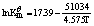
(1)计算在573K时。反应的ΔrGƟm,ΔrHƟm温和ΔrSƟm。.
(2)若开始时用等量的I2和环戊烯混合;温度为573K,起始总压为100kPa,试求平衡后I2的分压。
(3)若起始压力为1000kPa.试求平衡后I2的分压。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


 2HI+环戊二烯,得到
2HI+环戊二烯,得到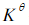 与温度(K)的关系为:
与温度(K)的关系为: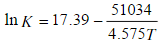
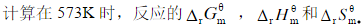
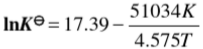 ,试计算:(1)在573K时反应的
,试计算:(1)在573K时反应的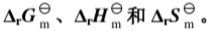 ;(2)若开始时用等物质的量的I2(g)和环戊烯(g)混合,温度为573K,起始总压为101.325kPa,达平衡后I2(g)的分压;(3)起始总压为1013.25kPa,达平衡后I2(g)的分压。
;(2)若开始时用等物质的量的I2(g)和环戊烯(g)混合,温度为573K,起始总压为101.325kPa,达平衡后I2(g)的分压;(3)起始总压为1013.25kPa,达平衡后I2(g)的分压。 2HI+环戊二烯,得到KpΘ与温度(K)的关系为:lnKpΘ=17.39一
2HI+环戊二烯,得到KpΘ与温度(K)的关系为:lnKpΘ=17.39一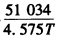 (1)计算在573K时,反应的△rGmΘ、△rHmΘ和△rSmΘ。 (2)若开始时用等量的12和环戊烯混合,温度为573K,起始总压为100kPa,试求平衡后12的分压。 (3)若起始压力为1000kPa,试求平衡后I2的分压。
(1)计算在573K时,反应的△rGmΘ、△rHmΘ和△rSmΘ。 (2)若开始时用等量的12和环戊烯混合,温度为573K,起始总压为100kPa,试求平衡后12的分压。 (3)若起始压力为1000kPa,试求平衡后I2的分压。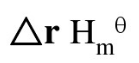 =-49.45kJ·mol-1。I2(s)在熔点113.5℃熔化时吸热16.7kJ·mol-1。I2(1)在沸点184.3℃,0.1MPa下蒸发时吸热42.7kJ·mol-1。在18~113℃区间Cp,m(I2,s)=55.6J·K-1·mol-1,在13.5~184.3℃区间Cp,m(12,1)=62.8J·K-1·mol-1,在184.3~200℃区间Cp,m(I2,g)=(35.56-5.4×10-3T/K)J·K-1·mol-1,在18~200℃区间Cp,m(H2,g)=(29.08-0.84×10-3T/K)J·K-1·mol-1,Cp,m(HI,g)=(28.07-2.1×10-3T/K)J·K-1·mol-1。求在200℃时,反应H2(g)+I2(g)===2HI(g)的
=-49.45kJ·mol-1。I2(s)在熔点113.5℃熔化时吸热16.7kJ·mol-1。I2(1)在沸点184.3℃,0.1MPa下蒸发时吸热42.7kJ·mol-1。在18~113℃区间Cp,m(I2,s)=55.6J·K-1·mol-1,在13.5~184.3℃区间Cp,m(12,1)=62.8J·K-1·mol-1,在184.3~200℃区间Cp,m(I2,g)=(35.56-5.4×10-3T/K)J·K-1·mol-1,在18~200℃区间Cp,m(H2,g)=(29.08-0.84×10-3T/K)J·K-1·mol-1,Cp,m(HI,g)=(28.07-2.1×10-3T/K)J·K-1·mol-1。求在200℃时,反应H2(g)+I2(g)===2HI(g)的 。
。


















