已知在18℃,0.1MPa下反应H2(g)+I2(g)→2HI(g)的=-49.45kJ·mol-1。I2(s)在熔点113.5℃熔化时吸热16.7kJ·mol-1。I2
已知在18℃,0.1MPa下反应H2(g)+I2(g)→2HI(g)的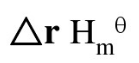 =-49.45kJ·mol-1。I2(s)在熔点113.5℃熔化时吸热16.7kJ·mol-1。I2(1)在沸点184.3℃,0.1MPa下蒸发时吸热42.7kJ·mol-1。在18~113℃区间Cp,m(I2,s)=55.6J·K-1·mol-1,在13.5~184.3℃区间Cp,m(12,1)=62.8J·K-1·mol-1,在184.3~200℃区间Cp,m(I2,g)=(35.56-5.4×10-3T/K)J·K-1·mol-1,在18~200℃区间Cp,m(H2,g)=(29.08-0.84×10-3T/K)J·K-1·mol-1,Cp,m(HI,g)=(28.07-2.1×10-3T/K)J·K-1·mol-1。求在200℃时,反应H2(g)+I2(g)===2HI(g)的
=-49.45kJ·mol-1。I2(s)在熔点113.5℃熔化时吸热16.7kJ·mol-1。I2(1)在沸点184.3℃,0.1MPa下蒸发时吸热42.7kJ·mol-1。在18~113℃区间Cp,m(I2,s)=55.6J·K-1·mol-1,在13.5~184.3℃区间Cp,m(12,1)=62.8J·K-1·mol-1,在184.3~200℃区间Cp,m(I2,g)=(35.56-5.4×10-3T/K)J·K-1·mol-1,在18~200℃区间Cp,m(H2,g)=(29.08-0.84×10-3T/K)J·K-1·mol-1,Cp,m(HI,g)=(28.07-2.1×10-3T/K)J·K-1·mol-1。求在200℃时,反应H2(g)+I2(g)===2HI(g)的 。
。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案



 CO2(g)+H2(g),将各气体视为理想气体,试计算:
CO2(g)+H2(g),将各气体视为理想气体,试计算:
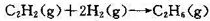
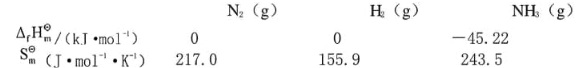 在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。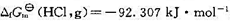 ,反应H2(g) +Cl2(g)→2HCl(g)在催化剂的作用下,可大大加快反应的速率,则此反应的
,反应H2(g) +Cl2(g)→2HCl(g)在催化剂的作用下,可大大加快反应的速率,则此反应的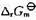 (298 K)为()
(298 K)为()


















