在723K时,将0.10 mol H2(g)和0.20 mol CO2(g)通入抽空的瓶中,发生如下反应:平衡后瓶中的总压为
在723K时,将0.10 mol H2(g)和0.20 mol CO2(g)通入抽空的瓶中,发生如下反应:
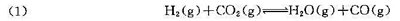
平衡后瓶中的总压为50.66kPa,经分析知其中水蒸气的摩尔分数为0.10.今在容器中加入过量的氧化钴CoO(s)和金属Co(s),在容器中又增加了如下两个平衡:
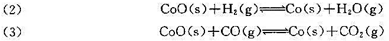
经分析知容器中的水蒸气的摩尔分数为0.30。试分别计算这三个反应用摩尔分数表示的平衡常数。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


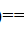 H2O(g)+CO(g)
H2O(g)+CO(g)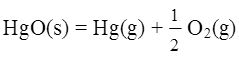 ,于693K达平衡时总压为5.16×104Pa,于723K达平衡时总压为1.08×105Pa,求HgO分解反应的
,于693K达平衡时总压为5.16×104Pa,于723K达平衡时总压为1.08×105Pa,求HgO分解反应的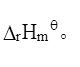 。
。
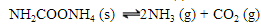 达平衡时,测得总压力为p,则反应的标准平衡常数
达平衡时,测得总压力为p,则反应的标准平衡常数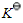 =______。
=______。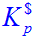 ,设气体为理想气体;
,设气体为理想气体;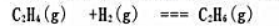
 在698K时,Kc=1.82×10-2,如果将HI(g)放人反应瓶中,试问:
在698K时,Kc=1.82×10-2,如果将HI(g)放人反应瓶中,试问: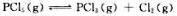 平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数
平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数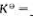 ().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。


















