A(g)+B(g) c(s)+Q(表示反应过程放出热量)对此反应来说,下列因素中哪些能影响它的反应速率()
A.温度
B.压强
C.生成物的浓度
D.生成物的物质的量
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
A.温度
B.压强
C.生成物的浓度
D.生成物的物质的量
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“A(g)+B(g) c(s)+Q(表示反应过程放出热量)对此…”相关的问题
更多“A(g)+B(g) c(s)+Q(表示反应过程放出热量)对此…”相关的问题
第1题
298.15K,反应A(s)+B(g)=C(g), =-41.8kJ·mol-1,B、C都是理想气体。反应在298.15K、标准状态下按下途径进行:体系做了最大功,放热1.67kJ·mol-1。则此过程的Q=______,W=______,
=-41.8kJ·mol-1,B、C都是理想气体。反应在298.15K、标准状态下按下途径进行:体系做了最大功,放热1.67kJ·mol-1。则此过程的Q=______,W=______,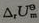 =______,
=______,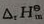 =______,
=______,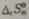 =______,
=______,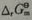 =______。
=______。
第2题
并放热4.86kJ.试求反应过程的Q、W、ΔrU、ΔrS和ΔrG。
第4题
A.Kp(I) =Kp (Ⅱ)
B.Kp(I) =Kp (Ⅱ)
C.O2(g)的平衡压力与计量方程的写法无关
D.Kp(Ⅰ) 随温度降低而减小。
第5题
在600K、100kPa压力下,生石膏的脱水反应为
CaSO4·2H2O(s)===CaSO4(s)+2H2O(g)
试计算该反应进度为1mol时的Q、W、△Um、△Hm、△Sm、△Am及△Gm。已知各物质在298K、100kPa的热力学数据如下表所示:
物质 | frac{Delta_{f}H_{m}^{Theta }}{kJcdot mol^{-1}} | frac{S_{m}^{Theta }}{Jcdot mol^{-1}cdot K^{-1}} | frac{C_{p,m}}{Jcdot mol^{-1}cdot K^{-1}} |
CaSO4·2H2O(s) | -2021.12 | 193.97 | 186.20 |
CaSO4(s) | -1432.68 | 106.70 | 99.60 |
H2O(g) | -241.82 | 188.83 | 33.58 |
第6题
A.热化学方程式中的反应物和生成物都必须注明状态
B.化学式前的系数是表示微粒的物质的量
C.方程式中表示热量数量前的“+”、“一”表示反应是“放出”还是“吸收”热量
D.“一131.3kJ”表示足够的红热的碳与lkg的水蒸气反应放出的热量为131.3kJ
第7题
植物在光合作用中合成葡萄糖的反应可以近似表示为:
6CO2(g)+6H2O(1)=C6H12O6(s)+6O2(g)
计算反应的标准摩尔吉布斯自由能,判断反应在298K及标准状态下能否自发进行,已知葡萄糖的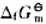 (C6H12O6·s) =-910.5kJ·mol-1。
(C6H12O6·s) =-910.5kJ·mol-1。
第10题
在723K时,将0.10mol H2(g)和0.20mol CO2(g)通入抽空的瓶中,发生如下反应:
(1) H2(g)+CO2(g)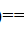 H2O(g)+CO(g)
H2O(g)+CO(g)
平衡后瓶中的总压为50.66kPa,经分析知其中水蒸气的摩尔分数为0.10。今在容器中加入过量的氧化钴CoO(s)和金属Co(s),在容器中又增加了如下两个平衡:
(2) CoO(s)+H2(g)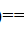 Co(s)+H2O(g)
Co(s)+H2O(g)
(3) CoO(s)+CO(g)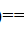 Co(s)+CO2(g)
Co(s)+CO2(g)
经分析知容器中的水蒸气的摩尔分数为0.30。试分别计算这三个反应用摩尔分数表示的平衡常数。


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧