题目内容
(请给出正确答案)
[主观题]
已知25℃时则标准状态下在酸性溶液中用过量铁粉还原Sn2+时,还原产物为();而用过量铁粉还
已知25℃时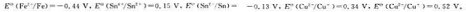 则标准状态下在酸性溶液中用过量铁粉还原Sn2+时,还原产物为();而用过量铁粉还原Cu2+时,还原产物为()。
则标准状态下在酸性溶液中用过量铁粉还原Sn2+时,还原产物为();而用过量铁粉还原Cu2+时,还原产物为()。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
已知25℃时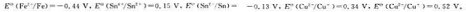 则标准状态下在酸性溶液中用过量铁粉还原Sn2+时,还原产物为();而用过量铁粉还原Cu2+时,还原产物为()。
则标准状态下在酸性溶液中用过量铁粉还原Sn2+时,还原产物为();而用过量铁粉还原Cu2+时,还原产物为()。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知25℃时则标准状态下在酸性溶液中用过量铁粉还原Sn2+时…”相关的问题
更多“已知25℃时则标准状态下在酸性溶液中用过量铁粉还原Sn2+时…”相关的问题
第2题
第3题
已知25℃时,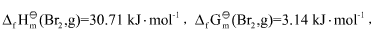 ,则Br2(l)的标准摩尔蒸发熵为______J·mol-1·K-1,正常沸点为______℃。
,则Br2(l)的标准摩尔蒸发熵为______J·mol-1·K-1,正常沸点为______℃。
第4题
向酸性的1.0×10-3mol·dm-3Fe3+溶液中加入过量液态汞,发生反应为:

第5题
甲烷燃烧过程可设计成燃料电池.当电解质为酸性溶液时,电极反应和电池反应分别为
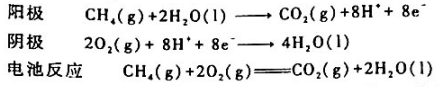
已知,25°C时有关物质的标准摩尔生成吉布斯函数 为
为
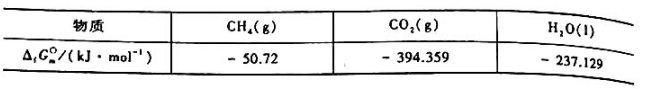
计算25°C时该电池的标准电动势.
第6题
已知下列电对的标准电极电势:
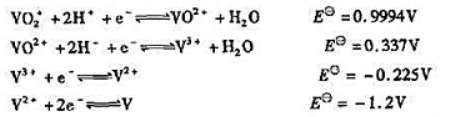
在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1Sn2+和Zn还原1.0mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?
第9题
A.0.2576V
B.0.279V
C.1.081V
D.1.777V
第10题
25℃时,Cu元素在酸性溶液中的元素标准电极电势图为
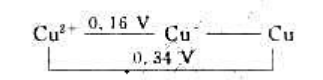
(1)试计算25℃时电对Cu2+/Cu的标准电极电势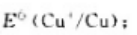
(2)已知2.303RT/F=0.060V,试计算25℃时Cu2+的歧化反应的标准平衡常数,
第11题


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧