题目内容
(请给出正确答案)
[主观题]
试计算压强为100 atm、密度为100 g/L的氧气的温度,已知氧气的范德瓦耳斯常量为a=1.360 atm·L²·mol-2,b= 0.03183L·mol-1.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“试计算压强为100 atm、密度为100 g/L的氧气的温度…”相关的问题
更多“试计算压强为100 atm、密度为100 g/L的氧气的温度…”相关的问题
第1题
把氧气当作范德瓦耳斯气体,它的范德瓦耳斯方程常量为a=1.36×10-1m6·Pa·mol-2,b=32×10-6m3·mol-1.试问压强为10.1MPa,密度为100kg·m-3的氧气的温度是多少?并把结果与氧气当作理想气体时的结果作比较.
第2题
第3题
第4题
对于CO2气体有范德瓦耳斯常量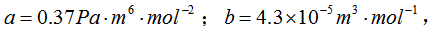 0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
0°C时其摩尔体积为6.0x10-4m3·mol-1。试求其压强。如果将其当作理想气体处理,结果又如何?
第5题
 。
。第7题
第9题
已知范徳瓦耳斯气体物恋方程为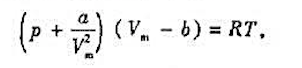
其内能为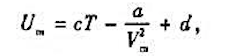
其中a,b,c,d均为常量。试求:(1)该气体从V1等温膨胀到V2时系统对外界所做的功;(2)该气体在定体下升高△T温度所吸收的热量。
第11题
一容器内贮有氧气,其压强为1.013×105Pa,温度为27℃。求:
(1)单位体积内的分子数;
(2)分子的平均平动动能;
(3)氧气的密度。
[玻尔兹曼常量k=1.38×10-23J/K,气体常量R=8.314J/(mol·K)]


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧