用旋转圆盘电极电解0.1mol·L-1CuSO4(有大量Na2SO4)溶液,圆盘电极面积为55cm2,转速为1转/秒,Cu2+的扩散系数
用旋转圆盘电极电解0.1mol·L-1CuSO4(有大量Na2SO4)溶液,圆盘电极面积为55cm2,转速为1转/秒,Cu2+的扩散系数为1.1×10-5cm2·s-1,溶液粘度为1.2×10-2g·cm-1·s-1,密度为1.1g·cm-3,求通过电极的极限电流。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
用旋转圆盘电极电解0.1mol·L-1CuSO4(有大量Na2SO4)溶液,圆盘电极面积为55cm2,转速为1转/秒,Cu2+的扩散系数为1.1×10-5cm2·s-1,溶液粘度为1.2×10-2g·cm-1·s-1,密度为1.1g·cm-3,求通过电极的极限电流。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“用旋转圆盘电极电解0.1mol·L-1CuSO4(有大量Na…”相关的问题
更多“用旋转圆盘电极电解0.1mol·L-1CuSO4(有大量Na…”相关的问题
第1题
A.2Cl-─→Cl2+2e-
B.Cu─→Cu2++2e-
C.Cu─→Cu++e-
D.2OH-─→H2O+O2+2e-
第2题
在0.1mol·L-1NaOH介质中,用阴极溶出伏安法测定S2-,以悬汞电极作为工作电极,在-0.40V时电解富集,然后溶出。分别写出富集和溶出时的电极反应式。
第3题
第4题
在锌电极上析出氢气的Tafel公式为
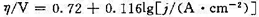
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
第5题
第6题
用电解沉积的办法分离Cd2+和Zn2+,已知H2在Cd上的超电势为0.48V,在Zn上的超电势为0.70V,溶液中的Cd2+和Zn2+浓度皆为0.1mol/kg。(已知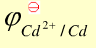 =-0.403V,
=-0.403V,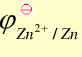 =-0.763V,离子的活度系数均为1,溶液的pH保持中性。)通过计算回答下面的问题:
=-0.763V,离子的活度系数均为1,溶液的pH保持中性。)通过计算回答下面的问题:
第7题
A.用该电池电解 CuCl2溶液,产生2.24L Cl2(标准状况)时,有0.1mol 电子转移
B.工作一段时间后,电解液中 KOH 的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.正极反应式为:O2+2H2O+4e-=4OH
第8题
在锌电极上析出氢气的Tafel公式为
η/V=0.72+0.116lg[j/(A·cm-2)]
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
第9题
X,Y,Z,W为原子序数依次增大的短周期元素,它们的最高价氧化物对应水化物分别为甲、乙、丙、丁,W的单质及某些化合物可用于自来水的消毒,常温下用0.1mol/L甲溶液滴定同浓度的20mL乙溶液,滴定曲线如图所示,甲、乙、丁均可与丙反应,下列说法正确的是()。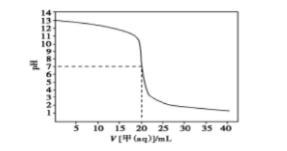
A.原子半径:W>Z>Y>X
B.简单氢化物的沸点:X
C.金属性Y>Z
D.Z,W所形成的化合物电解可冶炼Z


为了保护您的账号安全,请在“赏学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 赏学吧
赏学吧



 微信搜一搜
微信搜一搜
 赏学吧
赏学吧